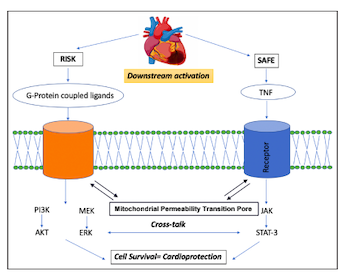
Il pomeriggio odierno in Sala dei Bastioni ha visto il susseguirsi di interessanti relazioni in tema di cardioprotezione e riduzione del danno miocardico in pazienti affetti da infarto miocardico acuto associato a sopraslivellamento del tratto ST (STEMI). I topics affrontati dai relatori hanno esplorato il ruolo del pre e post conditioning nella prevenzione e trattamento del danno da ischemia riperfusione, l’impiego delle terapie farmacologiche nel pretrattamento dell’infarto miocardico acuto e il ruolo dei sistemi percutanei di assistenza ventricolare temporanea nel management dei pazienti con STEMI complicato da shock cardiogeno. Il primo argomento è stato eviscerato nelle sue componenti dal dott. Filippo Ottani. Il danno da riperfusione è un fenomeno paradosso per cui, al momento della riperfusione coronarica, può aggiungersi al danno ischemico, ampliando di fatto l’infarct size e favorendo quindi l’evoluzione sfavorevole verso l’insufficienza cardiaca. Diversi e complessi sono i meccanismi fisiopatologici ipotizzati per la sua genesi: Romeo et al. hanno dimostrato il coinvolgimento di recettori mitocondriali, studiati in modelli animali ma attualmente privi di riproducibilità terapeutica negli esseri umani. Gli interventi di cardioprotezione in tal senso possono essere suddivisi in tre intervalli temporali: il precondizionamento che precede l’evento ischemico acuto, il peri-condizionamento, attuato nel contesto dello stesso, ed il post condizionamento, all’atto della procedura di riperfusione. Da queste definizioni risulta evidente come il pre condizionamento ischemico abbia scarse applicazioni pratiche data l’imprevedibilità dell’insorgenza di un infarto, mentre peri e, soprattutto, il post condizionamento siano stati ampio oggetto di studio. Tuttavia, studi osservazionali condotti nei primi anni dell’angioplastica coronarica hanno permesso di documentare come pazienti con IMA anteriore esteso preceduto da episodi di angina pre infartuale avessero delle infarct size inferiori rispetto a pazienti con IMA non preceduto da angina.
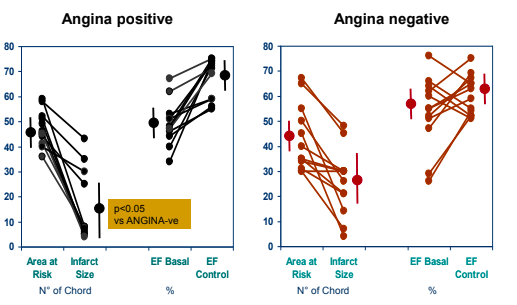
A partire da queste osservazioni sono stati condotti diversi studi sul post-condizionamento, anche remoto (ischemia transitoria indotta in altri distretti corporei, ad esempio al braccio tramite sfigmomanometro): il LIPSIA Conditioning Trial, il CONDI-2-ERC-PPCI hanno entrambi dato un risultato neutro e una metanalisi condotta da Xing et al ha confermato l’inefficacia di queste strategie nella prevenzione del danno da ischemia-riperfusione.
Maggiori sono le prospettive nella farmacologia del pretrattamento, come illustrato dal dott. De Luca. Le prime evidenze vengono da studi con gli inibitori GpIIb/IIIa: nello studio ON-TIME 2 l’aggiunta di Tirofiban ad aspirina e clopidogrel in pazienti candidati a PCI primaria ha ridotto in maniera significativa il rischio di morte, reinfarto e trombosi di stent, e importante è anche la tempistica in quanto i primi 45-60’ dall’esordio dei sintomi sono determinanti nel favorire l’ST-resolution mentre somministrazioni tardive ne riducono l’efficacia aumentando i sanguinamenti. Lo studio EUROMAX invece ha dimostrato che il trattamento con bivalirudina in fase preospedaliera nei pazienti trasportati per PCI primaria ha determinato un miglioramento dell’outcome clinico a 30 giorni oltre ad una riduzione del tasso di sanguinamenti maggiori, ma a fronte di un aumento di trombosi acuta dello stent. Diversa invece l’efficacia del pre treatment con inibitori orali P2Y12: lo studio di farmacocinetica FABOLUS-PRO ha mostrato come per avere un’inibizione significativa dell’aggregazione piastrinica con prasugrel vs tirofiban servano almeno 2 ore, con variabilità interindividuale che può raggiungere le 4-6 ore. Allo stesso modo, lo studio ATLANTIC ha dimostrato come la somministrazione di ticagrelor nel setting pre ospedaliero in pazienti con STEMI candidati a PCI sia sicura in termini di rischio emorragico ma non significativamente efficace nel migliorare la riperfusione coronarica pre PCI (intesa come riduzione di almeno il 70% dell’ST-up pre procedura).
Sono ancora diversi gli unmeet need in questo campo: tuttora circa il 20% dei pazienti con STEMI decede per arresto cardiaco extraospedaliero, mentre il 10% prima o nell’immediato post-procedura, da qui la necessità di trattamenti rapidi ed efficaci. A tal proposito è in fase di studio il selatogrel, P2Y12 inibitore altamente selettivo somministrato sottocute, con rapido esordio di azione e breve durata: lo studio SOS AMI arruolerà pazienti con una storia recente di infarto educati ad autoiniettarsi il prodotto per via sottocutanea, quando hanno sintomi sospetti di un nuovo infarto, valutandone end point di safety ed efficacia. L’ultima sessione ha visto lo studio dei sistemi di unloading ventricolare ai fini di ridurre il consumo di ossigeno, assistere la portata cardiaca, fornire bridge ed assistenza in corso di PCI high-risk in pazienti con STEMI complicato da shock cardiogeno. A tal proposito è stato approfondito il ruolo dell’IABP e dei sistemi Impella. L’IABP è ampiamente utilizzato tuttora vista la praticità del suo impiego, ma diverse sono le precisazioni da tener presente. Diversi studi hanno dimostrato come la risposta alla IABP sia diversa tra i pazienti con STEMI complicati da shock cardiogeno (IMA-CS) e i pazienti con scompenso cardiaco riacutizzato (ADHF-CS): nei secondi l’IABP è in grado di determinare un aumento della portata cardiaca in media di 5 volte superiore ai primi e, più di recente, l’IABP-SHOCK II ha portato all’indicazione per cui è attualmente in classe III l’impiego routinario dell’IABP nei pazienti con IMA-CS, mentre è in classe IIb qualora venga utilizzato come bridge o supporto. L’IMPELLA agisce invece come un dispositivo di assistenza ventricolare percutaneo, garantendo unloading e flusso continuo in aorta. Ne esistono di tipologie differenti classificate sulla base del flusso, del diametro del catetere, del diametro della pompa e del sito di inserzione; il più frequentemente impiegato è l’IMPELLA CP, in grado di fornire un flusso medio di 3.7 – 4.0 lpm, ed è utilizzato sia come bridge (to bridge vs to recovery) sia come supporto a procedure emodinamiche complesse e ad alto rischio. Dati dall’IMP-IT Registry hanno dimostrato come IMA-CS trattati con PCI, se supportati con IMPELLA prima della procedura esibiranno una miglior prognosi a breve e medio termine. Inoltre, sebbene il CULPRIT-SHOCK abbia ampiamente dimostrato come una rivascolarizzazione completa vs trattamento della culprit in pazienti IMA-CS non produca benefici significativi, la rivascolarizzazione completa di questi stessi pazienti in corso di supporto IMPELLA ne migliori invece la sopravvivenza. E’ pertanto postulato che l’unloading ventricolare, riducendo il mismatch richiesta/apporto di ossigeno, possa quindi impattare in maniera significativa sul danno di ischemia-riperfusione sopra descritto, riducendo notevolmente l’area di miocardio a rischio. Dalle sessioni presentate emerge quindi come quest’area, sebbene a tratti ancora oscura e per certi aspetti priva di opzioni terapeutiche efficace, meriti ulteriori studi ed approfondimenti per migliorare il trattamento della cardiopatia ischemica che, ancora oggi, rappresenta la prima causa di insufficienza cardiaca e di scompenso cardiaco avanzato.



