La sessione dedicata allo scompenso cardiaco a frazione di eiezione preservata (HFpEF) ha messo in luce come questa condizione rappresenti ancora una sfida clinica complessa che richiede un approccio multiparametrico. Il punto di partenza resta la diagnosi, spesso resa difficile dall’ambiguità dei sintomi, frequentemente attribuiti dai pazienti (e talvolta dai medici) all’invecchiamento o alla sedentarietà.
L’importanza della fenotipizzazione
Il Dott. Daniele Masarone ha ribadito la necessità di superare la semplice etichetta di HFpEF per identificare specifici “fenogruppi”. Pazienti con obesità, diabete, fibrillazione atriale o ipertensione polmonare rappresentano fenotipi distinti con prognosi e risposte terapeutiche differenti. Questa profilazione è fondamentale per guidare una terapia mirata, passando da un approccio empirico a una vera medicina di precisione. Un aspetto innovativo trattato da Masarone riguarda l’uso dell’intelligenza artificiale per identificare i “Phenogroups“. Attraverso algoritmi di machine learning, è possibile analizzare decine di variabili cliniche, ecocardiografiche e di laboratorio per raggruppare i pazienti in categorie con prognosi simile. Questo permette di identificare, ad esempio, il fenotipo “obeso-metabolico” (spesso caratterizzato da elevata infiammazione sistemica) rispetto al fenotipo “anziano-iperteso”. L’obiettivo della fenotipizzazione è prettamente operativo: garantire il farmaco giusto al paziente giusto. La ‘tabella di marcia’ di Masarone modula la terapia sul profilo clinico: per il fenotipo obeso/diabetico la priorità sono SGLT2i e GLP1-RA (come semaglutide) per agire sull’infiammazione del grasso epicardico; nei pazienti con fibrillazione atriale è cruciale il controllo del ritmo, inclusa l’ablazione; per chi presenta carenza di ferro, è indicato il carbossimaltosio ferrico. Infine, nell’ipertensione polmonare, la diagnosi differenziale tra forme pre e post-capillari resta il presupposto indispensabile per evitare approcci terapeutici inappropriati.
La diagnosi: tra clinica, flow-charts ed emodinamica da sforzo
Uno dei problemi centrali evidenziati è la “deception from symptoms” (l’inganno dei sintomi). Spesso la dispnea da sforzo viene erroneamente attribuita dal paziente o dal medico all’invecchiamento o alla sedentarietà, portando a un ritardo diagnostico. Parafrasando Eugene Braunwald, Caravita definisce l’HFpEF come una sindrome clinica derivante da alte pressioni di riempimento, che possono manifestarsi a riposo, oppure esclusivamente durante l’esercizio. Il percorso diagnostico proposto segue una struttura precisa per confermare il fenotipo HFpEF (FEVS ≥ 50%):
1) Sospetto clinico: Presenza di fattori di rischio, segni/sintomi e anomalie all’ECG.
2) Biomarcatori: NT-proBNP ≥125 pg/mL o BNP ≥35 pg/mL.
3) Ecocardiografia: Ricerca di anomalie morfo-funzionali (come l’ingrandimento dell’atrio sinistro o l’ipertrofia ventricolare).
Se i passaggi precedenti sono positivi, la diagnosi è confermata e si procede alla ricerca dell’eziologia e all’inizio del trattamento. Lo studio di Borlaug et al., 2010 evidenzia come nei casi dubbi, dove l’ecocardiografia a riposo non è conclusiva, sia utile l’esecuzione del cateterismo cardiaco destro da sforzo al cicloergometro. Mentre nei soggetti con dispnea non cardiaca la PCWP (wedge pressure) rimane stabile, nei pazienti con HFpEF precoce la PCWP sale drasticamente durante lo sforzo (superando i 25 mmHg al picco), smascherando la patologia. Per identificare i pazienti meritevoli di tale approfondimento, viene proposto come ausilio l’HFpEF-ABA score (Figure 1, 2).

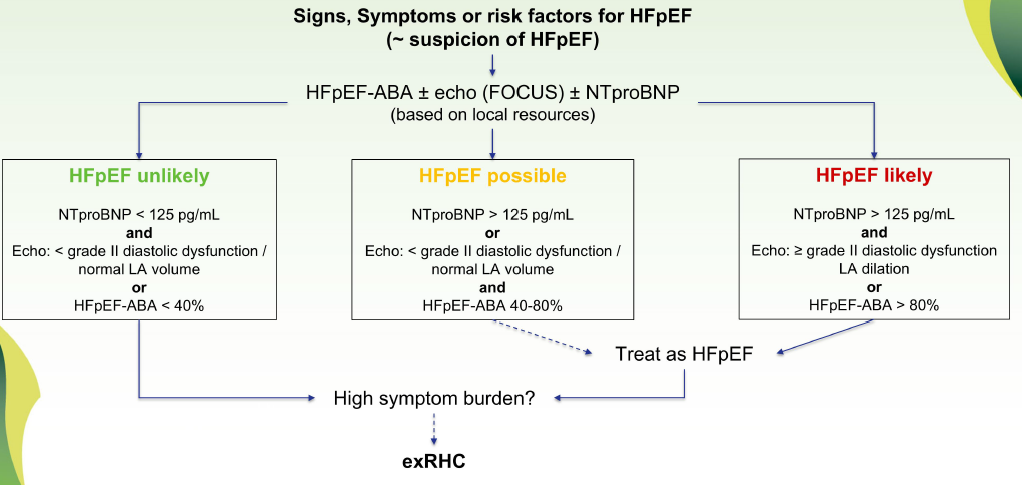
Il valore clinico di questo score risiede nella sua capacità di stratificare il rischio prima di procedere a esami più invasivi: un punteggio elevato indica una probabilità molto alta di HFpEF, guidando il clinico verso una conferma diagnostica e permettendo di superare quel “pregiudizio dell’età” che spesso porta a sottostimare i sintomi del paziente.
Le certezze terapeutiche di oggi e domani
In ambito terapeutico, il Dott. Andrea Passantino ha evidenziato come gli SGLT2 inibitori (empagliflozin e dapagliflozin) rappresentino oggi la classe con le evidenze più solide, capaci di ridurre significativamente le ospedalizzazioni per scompenso indipendentemente dallo stato diabetico o dall’indice di massa corporea. In ambito farmacologico, Passantino ha posto l’accento sull’evoluzione degli antagonisti del recettore dei mineralcorticoidi, segnalando il ruolo del finerenone. Questo MRA non steroideo si distingue per un profilo di sicurezza superiore e una maggiore selettività, offrendo una protezione cardio-renale efficace con un minor rischio di iperpotassiemia rispetto alle molecole tradizionali, posizionandosi come pilastro per il trattamento dei pazienti HFpEF col fenotipo cardio-renale. Altre opzioni promettenti includono, per il fenotipo obeso-metabolico, i GLP-1 receptor agonists come la semaglutide, che ha mostrato importanti miglioramenti nella qualità della vita e nella riduzione del peso corporeo. In conclusione, la gestione dell’HFpEF nel 2026 impone una diagnosi precoce e rigorosa, seguita da una caratterizzazione fenotipica dettagliata per applicare tempestivamente le terapie che oggi hanno un impatto reale sulla storia naturale della malattia.
Gestione del ritmo e frequenza cardiaca
L’intervento del Dott. Bartolini ha evidenziato come la gestione della frequenza cardiaca e del ritmo rappresenti uno dei nodi più complessi nella terapia dell’HFpEF a causa di meccanismi fisiopatologici radicalmente diversi rispetto all’HFrEF. Sebbene una frequenza cardiaca elevata sia un noto marker di rischio (associato a disfunzione endoteliale, aumento del consumo di ossigeno e progressione dell’aterosclerosi), nell’HFpEF la riduzione farmacologica della frequenza non ha dato i frutti sperati. I dati presentati indicano che a differenza dell’HFrEF, dove i beta-bloccanti sono un pilastro, nell’HFpEF questi farmaci non hanno mostrato benefici chiari sulla riduzione della mortalità: esiste il rischio concreto di peggiorare l’incompetenza cronotropa, che è una delle cause principali di intolleranza all’esercizio in questi pazienti. Riguardo le aritmie, la fibrillazione atriale è la “compagna di viaggio” più frequente dell’HFpEF (Figura 3).
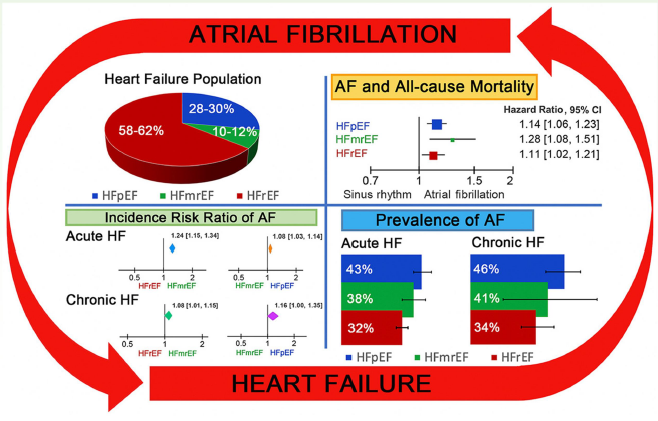
Bartolini ha sottolineato che la perdita del contributo atriale al riempimento ventricolare è drammatica in un cuore “rigido” (ipertrofico o fibrotico), per cui il mantenimento del ritmo sinusale appare preferibile rispetto al semplice controllo della frequenza, ricorrendo alla terapia antiaritmica o, in casi selezionati, all’ablazione transcatetere. Anche i disturbi della conduzione (come il blocco di branca sinistra) giocano un ruolo, sebbene meno codificato rispetto all’HFrEF. L’obiettivo futuro è identificare se specifici sottogruppi di pazienti con HFpEF possano beneficiare di terapie di resincronizzazione o di stimolazione fisiologica per ottimizzare il riempimento ventricolare. Il panorama del trattamento dello scompenso cardiaco a frazione di eiezione ridotta (HFrEF) sta vivendo un’accelerazione senza precedenti, spinta dalla necessità di rispondere a bisogni clinici ancora insoddisfatti nonostante i progressi farmacologici. La sessione ha affrontato il ciclo di vita della patologia, dalla gestione dell’episodio acuto fino alle fasi avanzate.
Titolazione e approccio “Quick-Start”
La Prof.ssa Aneta Aleksova ha delineato il cambio di paradigma nel trattamento dell’HFrEF, passando dalla storica cautela del ‘start low, go slow‘ alla strategia intensiva validata dallo studio STRONG-HF. Questo approccio impone una titolazione precoce dei ‘quattro pilastri’ (ARNI, beta-bloccanti, MRA e SGLT2i), da iniziare già durante il ricovero o subito dopo la dimissione, supportata da un monitoraggio stretto e frequente nelle prime settimane. Il percorso di cura viene pianificato attraverso quattro fasi – dalla diagnosi de novo alla gestione delle riacutizzazioni, fino all’ottimizzazione post-acuta – con l’obiettivo di raggiungere le dosi massime tollerate nel minor tempo possibile per abbattere il rischio di riospedalizzazione precoce. Un altro punto cardine sottolineato è stato il trattamento della carenza di ferro (spesso presente indipendentemente dall’anemia). Aleksova ha richiamato i dati dei trial IRONMAN e AFFIRM-AHF, ribadendo come la somministrazione endovenosa di carbossimaltosio ferrico sia fondamentale per ridurre le ospedalizzazioni.
La sfida del “Worsening Heart Failure”
Il Dott. Vito Altamura ha aperto i lavori focalizzandosi sul Worsening HF (WHF), che si definisce come un aggravamento dei sintomi e dei segni in un paziente con diagnosi nota di scompenso, che richiede un’intensificazione della terapia (tipicamente un aumento dei diuretici per via endovenosa o orale), anche in setting ambulatoriale o in pronto soccorso. Questo evento non è solo una tappa della progressione naturale, ma un marker prognostico severo: i pazienti ospedalizzati per WHF presentano una mortalità a un anno oltre 4,5 volte superiore rispetto a quelli stabili. Il rischio di morte a 30 giorni dopo un episodio di WHF ambulatoriale è paragonabile a quello di un paziente dimesso dopo un ricovero e la mortalità a un anno per chi subisce un peggioramento clinico è drammaticamente più alta rispetto ai pazienti stabili, rendendo questa fase una vera e propria “finestra di vulnerabilità” (Figura 4).
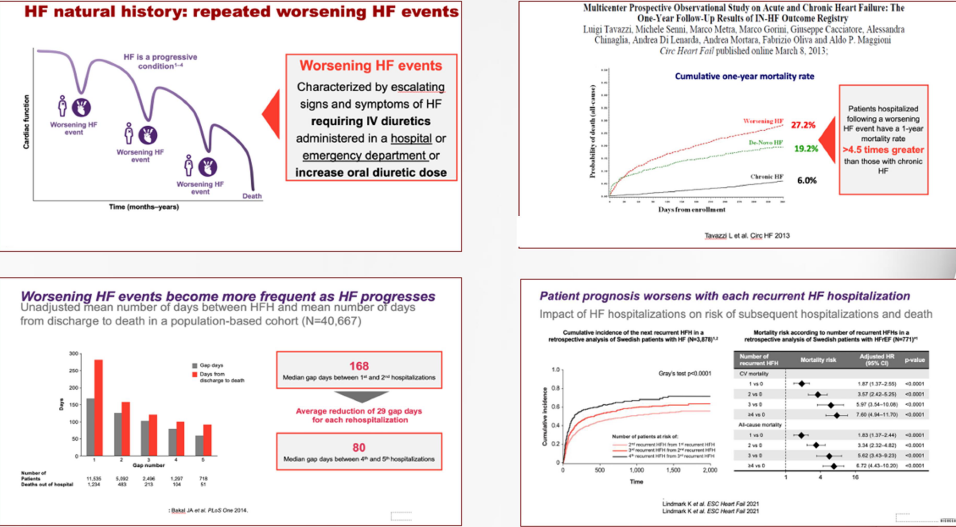
I meccanismi alla base del peggioramento spesso includono congestione residua persistente (sia emodinamica che clinica) e disfunzione d’organo progressiva. Per quanto riguarda l’approccio terapeutico, Altamura ha evidenziato due binari:
- farmacologico, ossia ottimizzare la quadruplice terapia e considerare l’introduzione del “quinto pilastro”, il vericiguat, che ha mostrato benefici significativi proprio nei pazienti con recente WHF;
- approccio non farmacologico: in questa fase è fondamentale rivalutare l’indicazione a terapie elettriche (CRT, CCM) o a interventi strutturali (come la riparazione della valvola mitrale nei casi di insufficienza funzionale severa), oltre a garantire un monitoraggio più stretto (telemedicina) per prevenire nuove riacutizzazioni.
L’era delle terapie elettriche: CRT e oltre
Sul fronte dei device, il Dott. Giovanni Bisignani ha illustrato come i dispositivi siano diventati parte integrante della gestione dello scompenso. Bisignani ha ribadito che i dispositivi non devono essere considerati come un’ultima spiaggia, ma come parte di un workflow strutturato. Dopo la diagnosi di HFrEF e una titolazione rapida della terapia farmacologica (3-6 mesi), è fondamentale rivalutare il paziente: se i sintomi persistono (NYHA ≥ II) e la frazione di eiezione resta ridotta, l’integrazione elettrica diventa necessaria. La CRT resta lo standard per correggere la dissincronia interventricolare, specialmente in presenza di blocco di branca sinistra (LBBB), come ribadito dalle Linee Guida. La stimolazione fisiologica (Conduction System Pacing – CSP) rappresenta invece una nuova frontiera. Bisignani ha illustrato come la stimolazione del fascio di His o della branca sinistra (LBBP) permetta un’attivazione elettrica del cuore molto più naturale rispetto alla stimolazione ventricolare tradizionale. Sono stati citati alcuni studi al riguardo: l’HeartSync-LBBP Trial ha dimostrato come l’LBBP sia superiore al pacing biventricolare nel ridurre il rischio di morte nei pazienti con LBBB e FE ridotta; nel PhysioSync-HF Trial invece la CSP non è riuscita a dimostrare la non inferiorità ed è risultata inferiore per un endpoint composito di mortalità per tutte le cause e ricoveri ospedalieri. A tal proposito, l’EHRA ha prodotto un documento di consenso per guidare la scelta tra le due metodiche descritte (Figura 5).
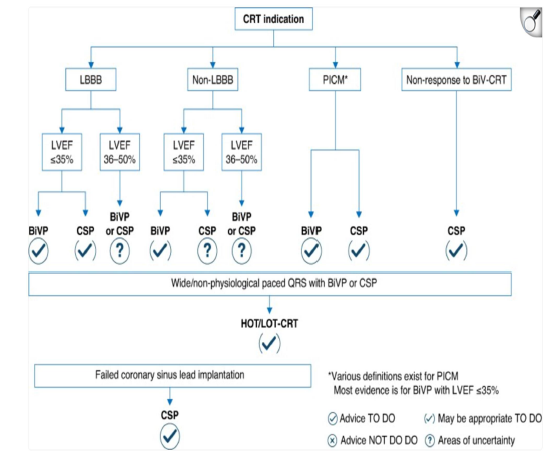
Un ampio spazio è stato dedicato alla CCM, una terapia specifica per i pazienti che non rispondono o non sono candidabili alla CRT (ad esempio con QRS stretto). Il dispositivo rilascia impulsi elettrici ad alta tensione durante il periodo refrattario assoluto del ciclo cardiaco. Non genera un battito, ma influenza la biologia del cardiomiocita, migliorando la gestione del calcio intracellulare e l’espressione genica. Target sono pazienti in NYHA III-IV, con frazione di eiezione compresa tra il 25% e il 45%. Infine, Bisignani ha evidenziato come i moderni dispositivi (ICD, CRT, CCM) fungano da veri e propri “sentinelle”. Grazie al monitoraggio remoto, è possibile intercettare precocemente aritmie o segni di congestione polmonare (attraverso sensori di impedenza), permettendo al clinico di intervenire prima che il paziente debba ricorrere al pronto soccorso.
La sfida ineludibile della palliazione
Infine, il Prof. Michele Emdin ha ribaltato il concetto di cure palliative: “Quando non c’è più niente da fare, c’è ancora molto da fare”. Emdin ha presentato i risultati della Survey Nazionale Intersocietaria, nata dalla collaborazione tra ANMCO e la Società Italiana di Cure Palliative (SICP). L’obiettivo è colmare il divario tra le necessità del paziente e l’attuale offerta assistenziale, integrando le competenze cardiologiche con quelle palliativistiche. La survey ha sottolineato l’importanza di avviare tempestivamente conversazioni sugli obiettivi di cura, permettendo di rispettare i desideri del paziente riguardo a interventi invasivi o alla gestione dei dispositivi (come gli ICD) e il punto di rottura rispetto al passato è il superamento della barriera temporale, per cui si parla di “cure simultanee”: le cure palliative non devono iniziare quando i trattamenti cardiologici falliscono, ma devono affiancarli precocemente lungo tutta la traiettoria della malattia avanzata, con l’obiettivo di gestire non solo il dolore, ma anche i sintomi refrattari tipici dello scompenso (dispnea, astenia, edemi) e il disagio psicologico e spirituale del paziente e della sua famiglia. Il Prof. Emdin ha ricordato e sottolineato che la medicina dello scompenso non è solo fatta di frazione di eiezione e biomarker, ma di comunicazione e relazione. Le strategie comunicative (come indicato nelle figure presentate sulla progressione della malattia) sono strumenti clinici a tutti gli effetti per supportare il paziente nel passaggio dalla terapia cronica al fine vita.


