Il Master ANMCO sulle Cardiopatie strutturali, moderato dai Dottori Claudio Fresco e Massimo Di Marco, ha aperto la sua prima sessione con la relazione del Dottor Corrado Lettieri afferente all’Ospedale Carlo Poma di Mantova, il quale ha presentato lo stato dell’arte relativo alle procedure di TAVI (Transcatheter Aortic Valve Implantation).
Partendo dalla presentazione dei risultati emersi da una metanalisi del 2019 di confronto dei livelli di rischio correlati a TAVI versus sostituzione valvolare aortica chirurgica (SAVR, surgical aortic valve replacement), con dati più a favore dell’approccio meno invasivo (Img.1. Fonte: European Heart Journal 2019 40, 3143-3153), è stata discussa l’importanza di una valutazione ponderata del rischio chirurgico e interventistico.
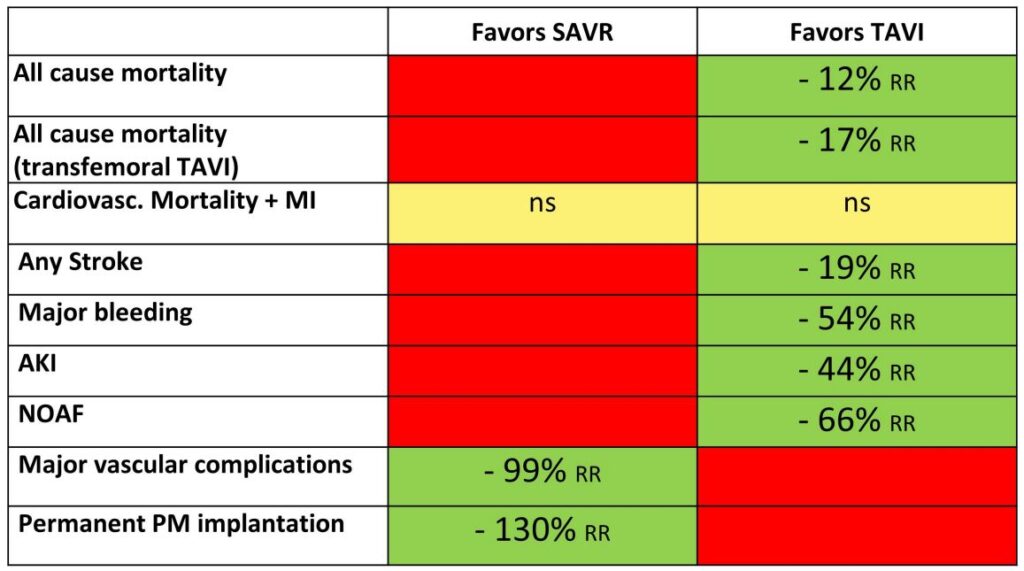
Le Linee Guida americane 2020 ed europee 2021 hanno stabilito i criteri di scelta della strategia terapeutica TAVI Vs SAVR, fra i quali riportiamo: valutazione del rischio chirurgico ed interventistico, età ed aspettativa di vita, caratteristiche cliniche, anatomiche e fattibilità tecnica, valutazione dell’Heart Team e preferenze del paziente (patient preference). In pazienti non ad alto rischio la preferenza del paziente (TAVI vs SAVR) deve essere considerata, come stabilito dalle Linee Guida AHA /ACC 2020, il dopo essere stato opportunamente informato del rapporto rischi-benefici derivanti. Al paziente deve esser data la possibilità di decidere tra due tecniche considerabili equipollenti scegliendo la procedura meno invasiva una volta informato opportunamente.
Stando alle suddette Linee Guida nei pazienti con difetti valvolari la procedura di TAVI è indicata in pazienti ad alto rischio con una classe I di raccomandazione. In pazienti non ad alto rischio è importante, invece, valutare il rapporto tra aspettativa di vita/età del paziente e la valve durability nota/ipotizzata. Generalmente più lunga è l’aspettativa di vita del paziente (età <75anni valore soglia) più è percorribile l’ipotesi del trattamento chirurgico piuttosto che percutaneo, dipendentemente dal caso clinico specifico. Nella scelta del trattamento più (SAVR) o meno invasivo (TAVI) il clinico dovrà tener conto delle caratteristiche cliniche e anatomiche del singolo paziente e della fattibilità tecnica, tenendo conto di eventuali specifici impedimenti. Sebbene raccomandata anche in pazienti a basso rischio chirurgico di età inferiore a 75 anni, sulla TAVI permangono alcune problematiche aperte quali: la durability limitata delle protesi transcatetere (seppur migliorata), eventuale riaccesso alle coronarie, PVL (Para Valvular Leak), % di impianto PM (seppur diminuita negli ultimi anni) e subset anatomici particolari (es. bicuspidia).
Sono stati inoltre presentati i risultati a medio termine (3-5 anni) di TAVI Vs SAVR dai quali è emersa la superiorità della TAVI sia in termini di mortalità per tutte le cause che di stroke o riospedalizzazione rispetto alla procedura chirurgica.
L’approccio cardiochirurgico è invece raccomandato dalle Linee Guida come primo approccio terapeutico nel paziente a basso rischio ed età inferiore a 75 anni. A tal proposito, sono stati presentati i dati relativi ai trend di utilizzo di TAVI e SAVR in USA, dal 2015 al 2021, in base alle diverse fasce d’età (Fonte: JACC 2022; 80: 2054-2056), dai quali è emerso come la TAVI venga effettivamente maggiormente eseguita nella fascia d’età avanzata: 65-80 anni nel 87.5% dei casi e e superiore a 80 anni nel 98.9% dei casi.
È stato infine ribadito il fondamentale ruolo dell’Heart Team di cardiochirurghi, specie in quei Centri non dotati di Cardiochirurgia e/o Chirurgia vascolare.
Di seguito (img 2) l’interessante slide di confronto TAVI vs Cardiochirurgia per il trattamento della stenosi aortica, dalla quale emergono chiaramente alcuni aspetti vantaggiosi dell’opzione TAVI.
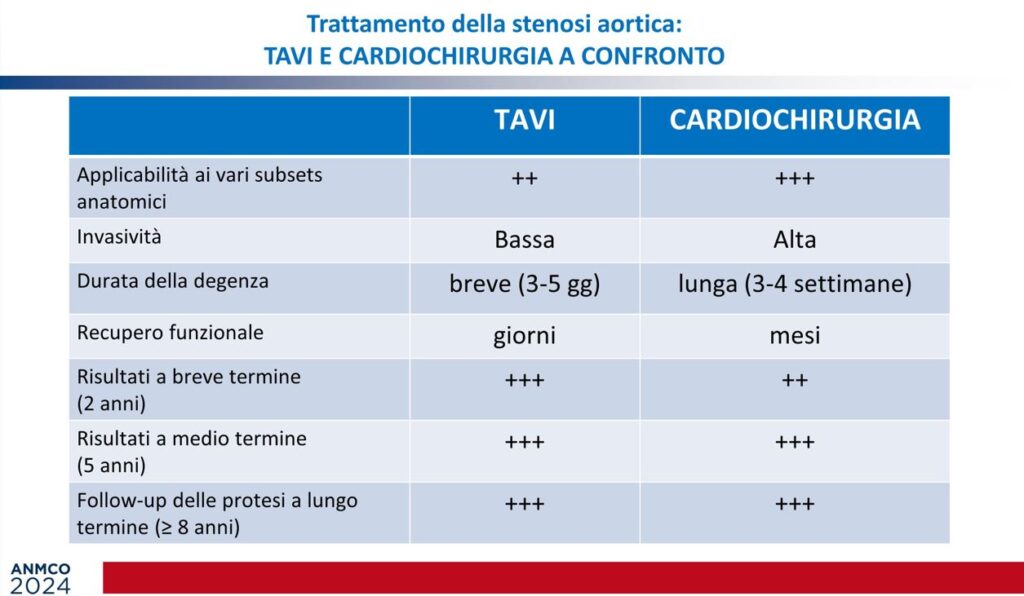
A seguire la relazione della Dottoressa Tiziana Attisano (A.O.U. San Giovanni di Dio e Ruggi di Salerno), che ha parlato di terapia antitrombotica con focus post-TAVI in diversi setting e del rischio di complicanze trombotiche e/o emorragiche nel paziente ad alto rischio (mortalità perioperativa) sottolineando come la medicina di precisione, improntata sull’ottimizzazione terapeutica individualizzata sul singolo paziente in base al profilo di rischio, valutando la DAPT (Dual AntiPlatelet Therapy), eventuale anticoagulazione con OAC, la procedura e la valvola.
Ha inoltre mostrato dei dati relativi all’aspirina in monoterapia, che a distanza di 3 mesi e 1 anno post TAVI, rispetto alla DAPT, si è dimostrata efficace proteggendo il paziente da eventi ischemici e trombotici, in assenza di complicanze emorragiche.
Ha altresì mostrato come l’associazione della terapia antitrombotica ad un anticoagulante non comporti un beneficio netto per il paziente sottoposto a TAVI, ma al contrario è generalmente causa di un aumento del rischio emorragico pur sottolineando la fondamentale rilevanza nella trombosi clinica (e non sub-clinica) con aumento di gradienti intraventricolare. Nel corso della relazione sono stati poi presentati i diversi algoritmi di trattamento, farmacologico e non, raccomandati nel paziente post-TAVI, illustrando casistiche particolari e scenari clinici specifici e concludendo riportanti gli attuali knowledge gaps in materia (e.g. introduzione e durata del trattamento terapeutico).
In successione poi la Dottoressa Katya Vitina Lucarelli (Ospedale F. Miulli di Acquaviva delle Fonti) che ha affrontato il trattamento percutaneo dell’insufficienza mitralica.
In classe IIa l’interventistica percutanea dell’insufficienza mitralica, questo grazie all’avanzamento tecnologico e ad un approccio sperimentale di base lungo 20 aa che ha portato alle attuali LG.
L’obiettivo non è solo quello di curare la valvola ma curare il paziente con il difetto valvolare nel pre-post procedurale comprendendo meglio la fisiopatologia e la conoscenza dell’apparato valvolare e dei meccanismi dell’insufficienza mitralica nella sua forma degenerativa (primaria) e funzionale (secondaria) e di tipo misto in cui i due meccanismi coesistono. Secondo la nota classificazione di Carpentier le forme degenerative sono il tipo I e II e quella funzionale sono il tipo III e IV.
Oggi possiamo intervenire sulla valvola mitralica sfruttando diversi device e tecniche:
Procedura Transcatheter Edge to Edge Repair, l’annuloplastica (diretta o indiretta), Transcatheter Mitral Valve Replacement. Come in altri ambiti restano delle questioni aperte non risolte. Dobbiamo selezionare bene il paziente e considerare come MitraClip non abolisce l’insufficienza valvolare ma la riduce e non si tratta di procedure prive di rischi e gravate da un certo tasso di complicanze per cui dobbiamo essere preparati ad affrontarli e risolverle. A questo proposito un ruolo centrale è il ruolo dell’imaging a supporto del cardiologo interventista.
In successione il Dottor Francesco Meucci ha esposto una presentazione sul trattamento percutaneo della insufficienza tricuspidale. L’insufficienza tricuspidalica è associata ad un’aumentata mortalità indipendentemente dalle pressioni polmonari e dalla funzione ventricolare destra.
Come per la mitrale si classificano in insufficienza tricuspidalica primaria, secondaria e terziaria
Nelle forme secondarie occorre distingue quelle da dilatazione atriale da quelle secondarie a dilatazione ventricolare. La differenza principale tra le due è che nelle forme atriali non è presente di norma il sovraccarico ventricolare destro e quindi sono quelle a prognosi migliore.
Ad oggi permangono molti knowledge gap. Dati tratti dal TRIVALVE registry in cui nel 68% dei casi è stato utilizzato un dispositivo per MitraClip ma in posizione tricuspidalica, il successo procedurale discriminava la prognosi. Inoltre, sono stati confrontati con un approccio propensity score matching, i pazienti del TRIVALVE registry con quelli di ampi registri in cui i pazienti con insufficienza tricuspidalica venivano trattati con terapia medica. Tale analisi ha mostrato come il trattamento percutaneo si associasse ad una migliore sopravvivenza.
Da questi primi dati incoraggianti è nato il triclip repair system che, senza necessità di attraversare il setto interatriale, permette di ridurre l’insufficienza tricuspidalica in maniera statisticamente significativa.
Il TRILUMINATE trial, pubblicato sul New England Journal of Medicine, ha arruolato pazienti per lo più con fibrillazione atriale, insufficienza tricuspidalica di tipo atriale con buona frazione di eiezione ventricolare sinistra e destra. Questo studio ha dimostrato come la prognosi e le ospedalizzazioni non sono state ridotte dal trattamento percutaneo, seppur con un miglioramento della qualità della vita, del distanza percorsa nel 6MWT e dell’insufficienza tricuspidalica. Il profilo di sicurezza della procedura è risultato buono con solo 3 eventi avversi maggiori pari all’1.7% delle procedure (un decesso e due casi di insufficienza renale acuta)
Sono in via di sviluppo nuovi device e una protesi in gradi sostituire la valvola tricuspide.
Come per la mitrale la selezione del paziente è essenziale: occorre tenere presente il tipo di vizio tricuspdalico, il rischio chirurgico, la fattibilità anatomica e lo stadio della patologia al momento della valutazione. Il candidato ideale è il paziente che rimane sintomatico nonostante la terapia diuretica, con funzione destra conservata o lievemente ridotta, senza ipertensione polmonare e con solo lieve depressione della funzione renale o epatica.
In occasione della discussione a chiusura della prima sessione interessanti le considerazioni affrontate sui dispositivi ad elevato impatto economico sul SSN, in un’ottica sempre più cost-effective e orientata alle preferenze del paziente informato.
La seconda parte della sessione del Master è stata moderata da Giancarlo Piovaccari e Sebastiano Quartuccio e si è aperta con la relazione del Dottor Pietro Martinucci (Ospedale S. Giovanni di Dio di Firenze) dal titolo “Chiusura percutanea dell’auricola sinistra: indicazioni e risultati”. Partendo da un breve inquadramento a livello epidemiologico mondiale (25% rischio generico di stroke nel corso della vita, con prevalenza dello stroke ischemico su quello emorragico), passando all’eziologia dello stroke (30% criptogenica; 20% cardioembolismo; 20% aterosclerosi; 25% lacune; 5% altro) e ai dati clinici (1/3 decesso in fase acuta, 1/3 disabilità residua e 1/3 disabilità lieve), è stato discusso il solido razionale dell’esclusione specifica dell’auricola sinistra e la tecnica di impianto LAAO (chiusura percutanea dell’auricola sinistra) in classe IIb di raccomandazione (cause irreversibili di emorragia cerebrale o fattori di rischio non modificabili) secondo le vigenti Linee Guida europee 2020.
Con l’aggiornamento delle Linee Guida americane (2023 ACC/AHA/ACCP/HRS) l’indicazione alla procedura di LAAO è progredita da IIA a II B ed è emersa, primariamente in via ufficiale, la dizione di “patient preference”: il paziente, cioè, deve essere messo a conoscenza delle terapie alternative (es. OAC) e deve poter scegliere.
Concetti chiave emersi in conclusione sono stati: la procedura di chiusura percutanea dell’auricola è una procedura sicura ed efficace; l’efficacia dell’intervento si esprime principalmente a carico delle complicanze emorragiche in corso di terapia anticoagulante; l’aderenza alla terapia anticoagulante è ancora un problema irrisolto; i risultati degli studi in corso forniranno evidenze più solide per definire le strategie terapeutiche nei pazienti con fibrillazione atriale non valvolare (FANV).
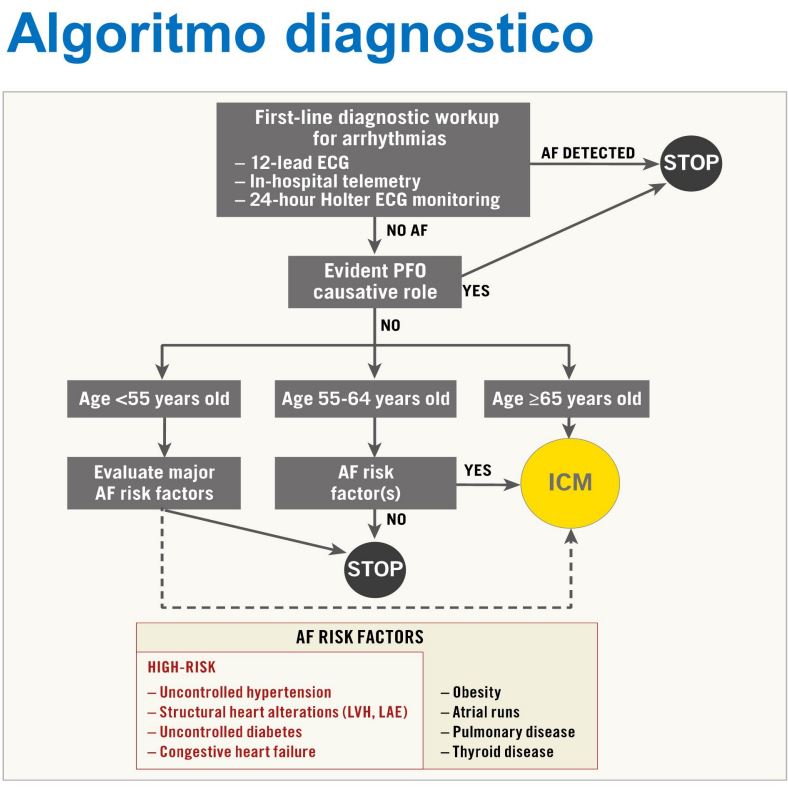
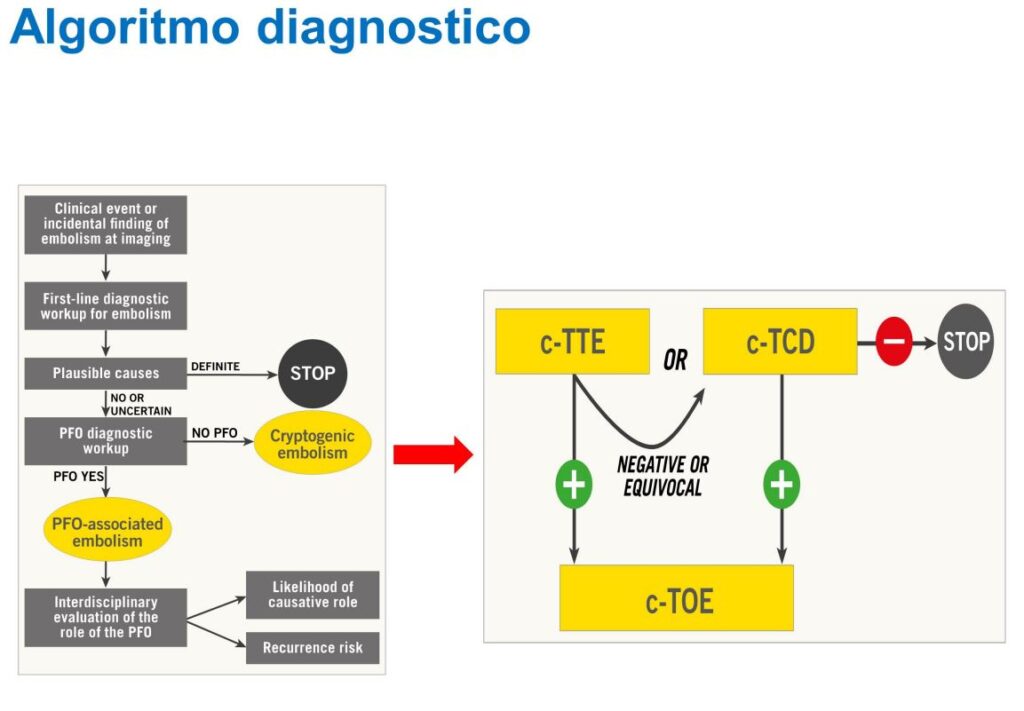
A seguire la relazione del Dottor Vittorio Pascale (P.O. Pugliese, Ciaccio – A.O.U. R. Dulbecco) che ha presentato le indicazioni al trattamento del Forame Ovale Pervio (PFO) partendo dalla sua definizione: comunicazione interatriale entro i confini della fossa ovale, funzionalmente e non anatomicamente chiusa, in assenza di una deficienza delle strutture intrinseche settali (Anderson R.H. Anat Rec 1996). Il PFO è dunque definibile come una variante anatomica presente nella popolazione che non impedisce lo shunt destro-sinistro con embolia paradosso per inversione pressoria. Sono state passate poi in rassegna le sindromi generalmente associate al PFO, quali lo stroke criptogenetico, la decompressione (spesso a eziologia professionale), l’emicrania e la deossigenazione arteriosa e la platypnea-ortho-deoxia (condizione in cui la chiusura del PFO è raccomandata). Sono state inoltre esposte le evidenze emerse dai clinical trials condotti nell’ambito e il risultante algoritmo diagnostico raccomandato (img 3 e 4 by Pristipino et al., EuroIntervention 2019; 14: 1389-1402), per stratificare correttamente il paziente escludendo cause diverse dal PFO e poterlo candidare ad un trattamento interventistico di chiusura percutanea. Sono stati infine riportati riferimenti alle Linee Guida AHA/ASA 2021 per la prevenzione dello stroke, in pazienti ad alto rischio con stroke o TIA (Transient Ischemic Attack), dalle quali emerge una classificazione IIa di raccomandazione relativa al PFO.
A concludere la seconda sessione una relazione sul trattamento percutaneo dei leak paravalvolari (PVL) della Dottoressa Giovanna Erente (Ospedale di Vicenza).
I ParaValvular Leak (PVL) sono rigurgiti dovuti al passaggio di sangue tra la valvola e la struttura anatomica che costituisce l’anello valvolare.
La chiusura dei PVL segue la flow-chart rappresentata in figura (img 5)
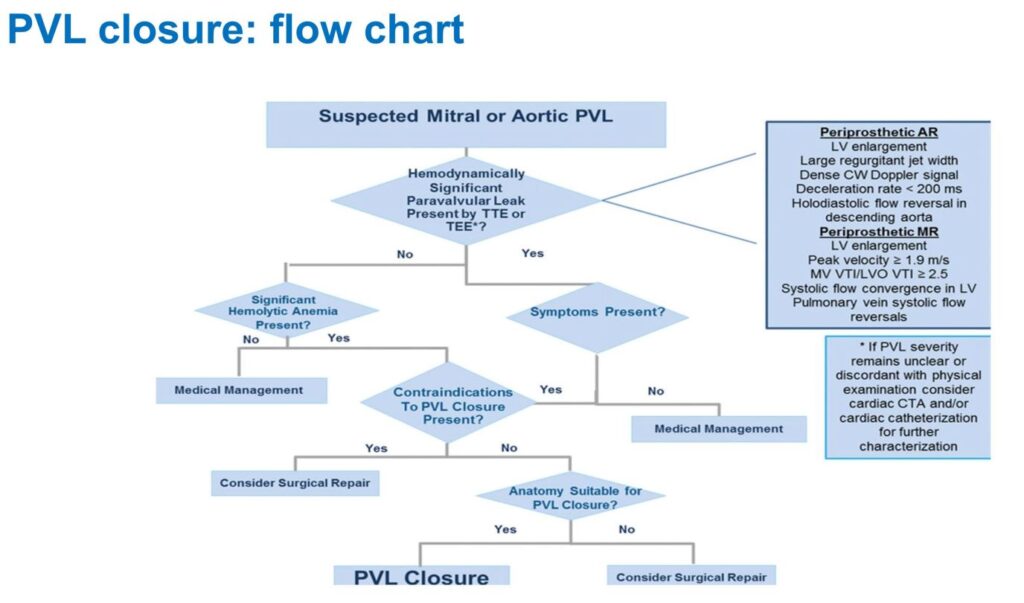
Gli outcome della procedura sono buoni solo se la procedura ha un buon risultato. Infatti, la sopravvivenza è correlata al fallimento procedurale. L’outcome a lungo termine dipende anche dalla classe NYHA residua.
È stata poi offerta una breve panoramica sui devices attualmente più in uso.
Come per tutte le procedure strutturali l’ecocardiogramma tranesofageo pre-procedurale è fondamentale per la diagnostica, la scelta del device (sizing, in funzione del difetto osservato) e approccio procedurale per il trattamento percutaneo (transaortico, transettale). Presentazione conclusiva di procedure complessa di chiusura Leak mitralico e meno complessa di chiusura leak aortico.
Obiettivo: fare in modo che il rigurgito residuo rimanga il minore possibile.
Nell’arco della sessione è stato infine introdotto, e portato poi avanti a più riprese da diversi relatori, il concetto di “medicina di precisione” in termini di trattamento sempre più personalizzato e mirato (“patient-tailored” appunto) che tenga conto delle differenze individuali.


