La miocardite acuta rappresenta una delle sindromi cardiovascolari più eterogenee e imprevedibili della pratica clinica contemporanea. Se molti pazienti vanno incontro a completa guarigione clinica e strumentale, una quota significativa sviluppa eventi aritmici maggiori, disfunzione ventricolare persistente o progressione verso fenotipi cardiomiopatici. La vera sfida non è più soltanto gestire la fase acuta, ma identificare precocemente quali pazienti manterranno un rischio residuo di morte cardiaca improvvisa nel medio-lungo termine.
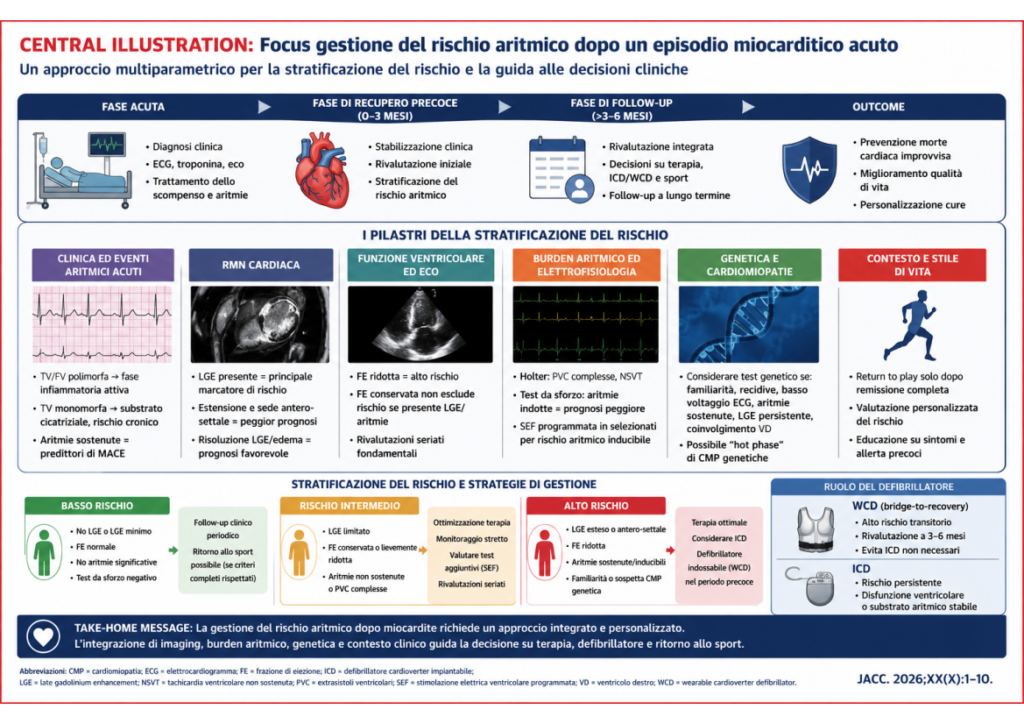
Negli ultimi anni la comprensione fisiopatologica della miocardite è profondamente cambiata. Il rischio aritmico non dipende esclusivamente dall’infiammazione acuta, ma dall’interazione tra edema, danno miocardico, rimodellamento elettrico e sviluppo di fibrosi. Le aritmie ventricolari osservate nella fase iniziale non hanno infatti tutte lo stesso significato prognostico. Tachicardia ventricolare polimorfa e fibrillazione ventricolare riflettono più spesso una fase infiammatoria attiva e instabile, mentre la tachicardia ventricolare monomorfa suggerisce frequentemente la presenza di un substrato cicatriziale organizzato e quindi di un rischio cronico di recidiva.
I registri più recenti confermano che i pazienti con miocardite complicata da aritmie ventricolari sostenute presentano una prognosi peggiore rispetto alle forme non aritmiche. In particolare, la presenza di tachicardia ventricolare monomorfa si associa a un incremento significativo del rischio di recidive aritmiche e MACE durante follow-up prolungato. In alcune coorti il tasso di eventi aritmici maggiori supera il 40% a distanza di pochi anni dall’episodio indice, dimostrando come il rischio non si esaurisca con la risoluzione della fase acuta.
In questo contesto, la risonanza magnetica cardiaca ha assunto un ruolo centrale nella stratificazione prognostica. La presenza di late gadolinium enhancement (LGE) rappresenta oggi uno dei principali marker di rischio, indipendentemente dalla frazione di eiezione. Estensione e localizzazione del LGE influenzano significativamente l’outcome: il coinvolgimento antero-settale e i pattern estesi di fibrosi si associano a maggiore rischio di morte cardiaca improvvisa, arresto cardiaco rianimato, shock appropriati ICD e ospedalizzazioni per scompenso.
Anche nei pazienti con frazione di eiezione conservata la persistenza di fibrosi miocardica identifica un sottogruppo non completamente guarito. Al contrario, la regressione di edema e LGE alla RMN di controllo si associa a prognosi favorevole e può consentire nel tempo una riduzione della terapia antiaritmica nei soggetti senza burden aritmico residuo.
La frazione di eiezione ventricolare sinistra mantiene comunque un importante valore prognostico. I pazienti con FE ridotta presentano maggiore incidenza di eventi ventricolari sostenuti e outcome peggiori. Tuttavia, il solo parametro funzionale non è sufficiente a definire il rischio reale. Esistono infatti pazienti con FE conservata ma marcata fibrosi o aritmie ventricolari complesse, così come soggetti con severa disfunzione iniziale che mostrano progressivo recupero durante follow-up e ottimizzazione terapeutica.
Per questo motivo cresce l’interesse verso una stratificazione multiparametrica che integri imaging, elettrofisiologia e valutazione funzionale. Holter ECG, test da sforzo e stimolazione ventricolare programmata possono contribuire a identificare pazienti ad alto rischio. La persistenza di extrasistolia ventricolare complessa o aritmie inducibili rappresenta un elemento prognostico sfavorevole e può modificare le decisioni terapeutiche.
Particolarmente delicato è il tema del return to play nel paziente sportivo. L’esercizio intenso può amplificare instabilità elettrica e trigger adrenergici in un miocardio non completamente guarito. Le attuali raccomandazioni suggeriscono sospensione dell’attività agonistica per almeno 3-6 mesi dopo miocardite acuta. Il ritorno allo sport dovrebbe essere consentito solo dopo remissione clinica e strumentale completa: assenza di sintomi, normalizzazione di troponina ed ECG, assenza di aritmie ventricolari a Holter e test ergometrico, oltre a RMN senza segni di infiammazione attiva.
Un altro aspetto emergente riguarda la sovrapposizione tra miocardite e cardiomiopatie genetiche, in particolare nelle cosiddette “hot phases” aritmogene. Varianti patogenetiche di geni desmosomiali, come DSP o PKP2, possono manifestarsi con dolore toracico, rialzo troponinico e quadro simil-miocarditico. Familiarità per morte improvvisa, episodi ricorrenti, basso voltaggio ECG, aritmie ventricolari sostenute e persistenza o progressione del LGE devono orientare verso approfondimento genetico.
Anche il ruolo del defibrillatore è oggi più articolato rispetto al passato. Nella fase precoce il defibrillatore indossabile rappresenta una strategia sempre più utilizzata come bridge-to-recovery nei pazienti con elevato rischio transitorio di morte improvvisa. Questa soluzione consente di proteggere il paziente durante la fase di recupero e rivalutare successivamente funzione ventricolare, burden aritmico e substrato RMN, evitando impianti ICD non necessari.
Le indicazioni all’ICD definitivo devono quindi basarsi su una valutazione globale che consideri timing clinico, persistenza di disfunzione ventricolare, substrato fibrotico, storia aritmica e profilo genetico. La gestione moderna del rischio aritmico post-miocardite richiede oggi un approccio integrato e personalizzato, capace di combinare clinica, imaging avanzato, elettrofisiologia e genetica per guidare prognosi e trattamento.


