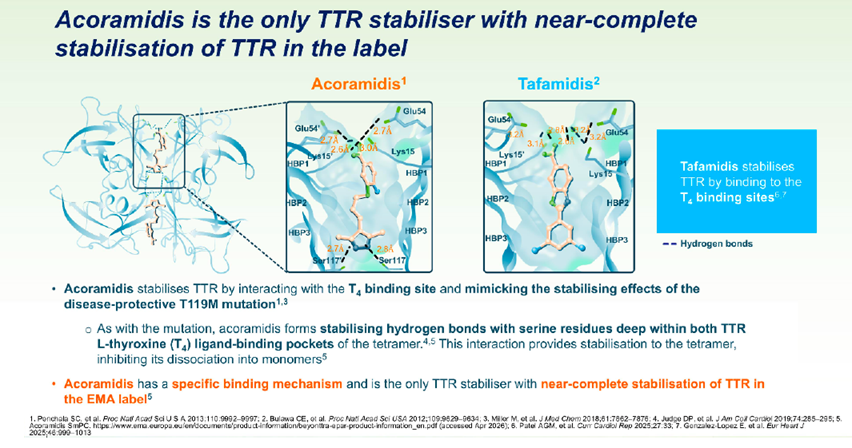
Lo scompenso cardiaco rappresenta oggi uno dei principali ambiti di innovazione della cardiologia clinica. La crescente consapevolezza della complessità del paziente cardio-renale-metabolico e il riconoscimento sempre più precoce dell’amiloidosi cardiaca stanno infatti modificando profondamente l’approccio terapeutico e organizzativo. La gestione dello scompenso non può più essere considerata limitata esclusivamente alla funzione ventricolare. Il paziente con insufficienza cardiaca presenta frequentemente un’interazione dinamica tra cuore, rene e metabolismo, con diabete, insufficienza renale cronica e infiammazione sistemica che contribuiscono alla progressione della malattia e all’aumento del rischio residuo. In questo contesto si inserisce il ruolo di vericiguat, stimolatore della guanilato ciclasi solubile, sviluppato per agire sul pathway ossido nitrico–cGMP, frequentemente alterato nei pazienti con scompenso avanzato. Lo studio VICTORIA ha dimostrato, nei pazienti con Worsening Heart failure e fenotipo HFrEF, una riduzione significativa del composito di morte cardiovascolare e ospedalizzazione per scompenso rispetto al placebo, soprattutto in una popolazione ad elevato rischio clinico. Il dato assume particolare rilevanza perché ottenuto in pazienti già trattati con terapia medica ottimizzata, evidenziando quindi un beneficio additivo nelle fasi più vulnerabili della malattia. Accanto alla modulazione neuro-ormonale, crescente interesse è rivolto al ruolo dell’asse cardio-renale-metabolico e dell’infiammazione fibrotica. In questo scenario finerenone, antagonista non steroideo del recettore dei mineralcorticoidi, ha dimostrato di ridurre progressione renale ed eventi cardiovascolari nei pazienti con diabete tipo 2 e nefropatia cronica negli studi FIDELIO-DKD e FIGARO-DKD. Più recentemente, il trial FINEARTS-HF ha esteso il potenziale impatto clinico di finerenone anche ai pazienti con frazione di eiezione lievemente ridotta o preservata, mostrando una riduzione degli eventi di worsening heart failure e morte cardiovascolare. Si consolida così il concetto di una terapia capace di intervenire simultaneamente sui meccanismi di congestione, fibrosi, infiammazione e progressione cardio-renale. Se il paradigma cardio-renale-metabolico rappresenta una delle principali evoluzioni dello scompenso, l’amiloidosi cardiaca costituisce probabilmente il modello più emblematico di trasformazione diagnostica e terapeutica degli ultimi anni. Un tempo considerata patologia rara e sostanzialmente priva di opzioni terapeutiche efficaci, l’ATTR-CM è oggi riconosciuta come causa non infrequente di scompenso cardiaco nell’anziano, soprattutto nei pazienti con ipertrofia ventricolare apparentemente “incongrua”, stenosi aortica, fibrillazione atriale o sindrome del tunnel carpale. Nonostante la maggiore sensibilità culturale, il ritardo diagnostico rimanga ancora rilevante: molti pazienti ricevono la diagnosi dopo anni di sintomi e ripetute ospedalizzazioni. Tale ritardo è particolarmente critico poiché la progressione dell’accumulo amiloide determina deterioramento funzionale, riduzione della qualità di vita e aumento della mortalità. Dal punto di vista fisiopatologico, la destabilizzazione della transtiretina rappresenta il momento chiave della malattia: la dissociazione del tetramero favorisce il misfolding proteico e la deposizione di fibrille amiloidi nel miocardio. In questo contesto si inserisce acoramidis, stabilizzatore della transtiretina progettato per mimare la mutazione protettiva T119M e ottenere una quasi completa stabilizzazione della proteina (Figura 1).
Lo studio ATTRibute-CM ha rappresentato un passaggio fondamentale nell’evoluzione terapeutica dell’ATTR-CM. Nei pazienti trattati con acoramidis è stata osservata una significativa riduzione del rischio combinato di mortalità per tutte le cause e ospedalizzazioni cardiovascolari ricorrenti a 30 mesi, associata a miglioramento o rallentamento del declino funzionale, dei livelli di NT-proBNP e della qualità di vita misurata mediante KCCQ. Di particolare interesse risultano inoltre i dati di estensione open-label fino a 54 mesi, che suggeriscono persistenza del beneficio clinico nel tempo, con riduzione progressiva della mortalità cardiovascolare e mantenimento della stabilizzazione biologica della transtiretina. Appare chiaro come l’innovazione nello scompenso cardiaco non riguarda soltanto nuovi farmaci, ma un cambiamento culturale dell’intero percorso assistenziale. Diagnosi precoce, stratificazione fenotipica, integrazione cardio-renale-metabolica e medicina di precisione stanno progressivamente ridefinendo la pratica clinica quotidiana. In questo scenario, terapie come vericiguat, finerenone e acoramidis rappresentano non semplicemente nuove opzioni farmacologiche, ma strumenti concreti per modificare la storia naturale della malattia e migliorare sopravvivenza, autonomia funzionale e qualità di vita dei pazienti.


